1. Akut koronart syndrom
1.1 Definition
Akut koronart syndrom (AKS) inddeles i:
- akut myokardieinfarkt (AMI) med ST-segment elevation i EKG (STEMI)
- AMI uden ST-segment elevation i EKG (NSTEMI)
- ustabil angina pectoris (UAP)
AMI defineres ud fra følgende kriterier:
1) stigning og/eller fald i kardial troponin (se Afsnit 1.4)
og
2) holdepunkter for akut myokardieiskæmi med mindst et af følgende:
- symptomer på akut iskæmi (f.eks. brystubehag og/eller dyspnø/akut hjertesvigt og/eller arytmier), jf. Kapitel 40. Akutte hjertesygdomme: Visitation og Differentialdiagnostik
- EKG-forandringer tydende på akut iskæmi (nye ST-T ændringer eller grenblok), jf. nedenfor
- udvikling af Q-takker i EKG’et
- billeddiagnostisk holdepunkt for nyt tab af viabelt myokardium eller ny regional dyskinesi med et mønster foreneligt med iskæmisk ætiologi
- påvisning af intrakoronar trombe ved angiografi eller obduktion
For uddybende beskrivelse af typeinddelingen af AMI, se Appendix 1.1.
Ustabil angina pectoris (UAP):
UAP er karakteriseret ved:
- symptomer på myokardieiskæmi opstået under hvile eller ved minimal fysisk udfoldelse
- crescendo angina pectoris med stigning i anfaldsfrekvens og varighed hos patienter med forud bestående kronisk koronart syndrom
UAP er en klinisk diagnose, som stilles på baggrund af anamnesen. Forbigående EKG-forandringer støtter diagnosen og har prognostisk betydning, men er ikke obligatoriske. Troponinværdier er ikke signifikant forhøjede, da tilstanden ellers klassificeres som NSTEMI.
Differentialdiagnoser skal overvejes, særligt ved ukarakteristiske symptomer. Det vigtigste i den akutte situation er at skelne AKS fra andre livstruende tilstande som aortadissektion, lungeemboli, pneumothorax og øvre gastrointestinale lidelser.
1.2 Akut udredning
EKG optages umiddelbart og før al anden diagnostik, optimalt præhospitalt. Der optages kort anamnese med fokus på tidspunkt for symptomdebut, prodromer, varighed og karakter af symptomer samt risikofaktorer for udvikling af iskæmisk hjertesygdom. jf. Kapitel 40: Akutte hjertesygdomme: Visitation og differentialdiagnostik.
Overvej straks, om der er indikation for akut KAG.
Ved inkonklusivt EKG eller forværrede/fortsatte symptomer gentages EKG med korte intervaller (hvert 10. minut), indtil diagnostisk afklaring er nået. Overvej supplerende EKG optagelse sv.t. afledning V7-V9 og V3R-V4R (se nedenfor). I tvivlstilfælde konfereres med primær PCI center.
1.2.1 EKG
STEMI
- ny ST-segment elevation i J-punktet i mindst 2 samhørende EKG-afledninger:
- V2-3: ≥0,25 mV hos mænd under 40 år; ≥0,20 mV hos mænd på/over 40 år, ≥0,15 mV hos kvinder
- øvrige afledninger ≥0,1 mV
- patienter med venstresidigt grenblok (kendt eller nyopstået), højresidigt grenblok med ledsagende ST-segmentforandringer forenelige med akut myokardieiskæmi eller ventrikulær pacerytme kan udgøre en diagnostisk udfordring, og ved klinisk mistanke om pågående myokardieiskæmi bør akut KAG overvejes. Ved venstresidigt grenblok eller ventrikulær pacerytme kan modificerede Sgarbossakriterier støtte mistanken om kritisk koronarstenose eller okklusion, se Figur 1.1.
- tegn på hovedstamme-/flerkarssygdom (ST-segment elevation i aVR og/eller V1 med samtidig ST-segment depression i ≥6 afledninger)
- tegn på ’posteriort’ STEMI (ST-segment depression i V1-4, evt. med non-signifikant ST-segment elevation i II, III og aVF). Overvej supplerende optagelse sv.t. V7-V9 hvor grænsen for ST-segment elevation er ≥0,05 mV
Der findes desuden en række karakteristiske EKG-forandringer uden klassisk ST-segment elevation, som kan ses ved kritisk koronarstenose/-okklusion, og som ved tilstedeværelse af relevante symptomer bør give anledning til konference med primær PCI center mhp. om, der er indikation for akut KAG. En oversigt over disse forandringer er vist i Figur 1.1.
NSTEMI/UAP
- ny ST-segment depression, horisontal eller descenderende ≥0,05 mV i to samhørende afledninger
- T-taks invertering >0,1 mV i to afledninger med prominent R tak eller R/S ratio >1
- en del patienter vil have uspecifikke EKG-forandringer eller normalt EKG
Figur 1.1: EKG mønstre der tyder på kritisk koronarstenose eller okklusion |
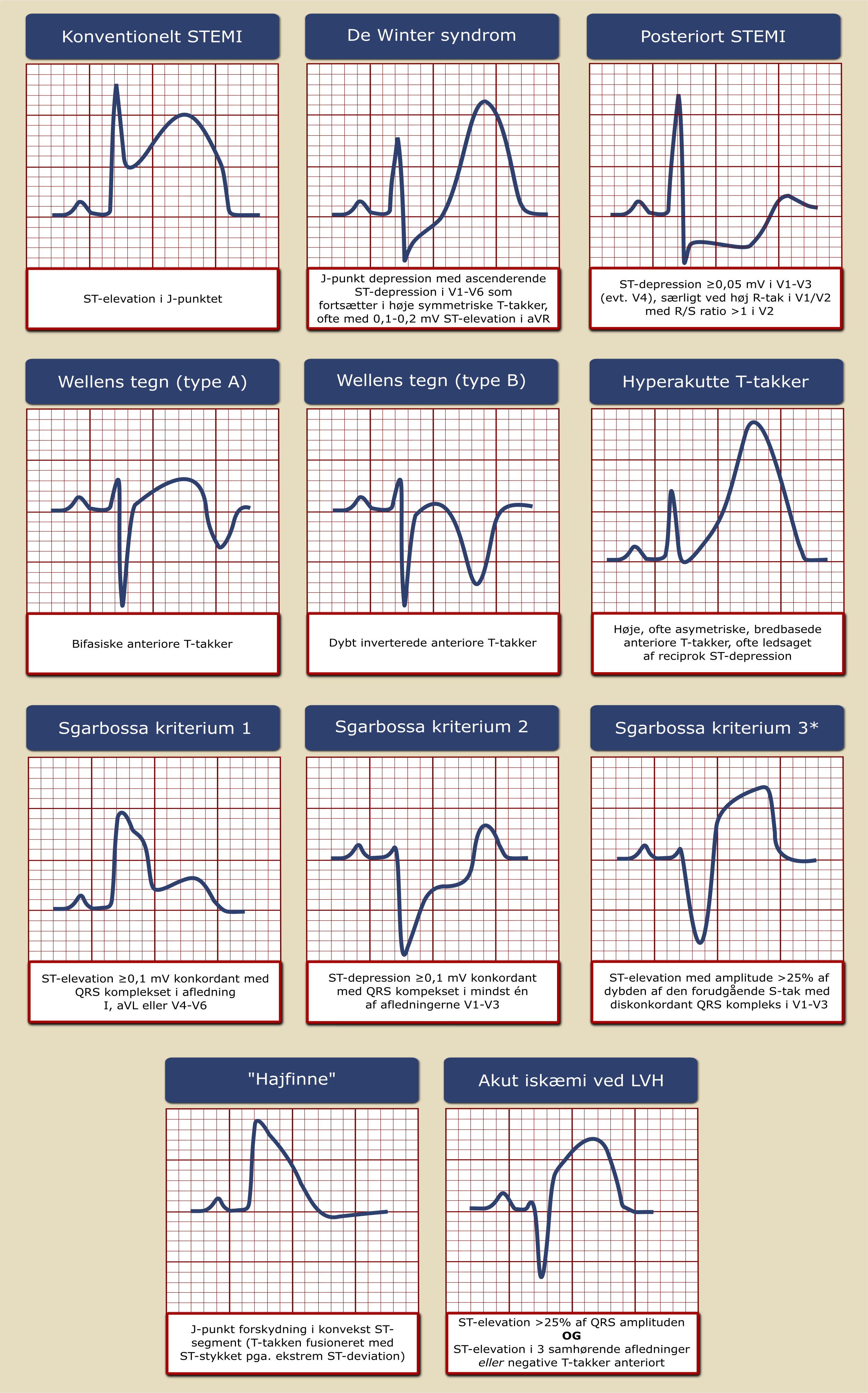 |
* Smith-modificerede Sgabossa kriterium LVH: Venstre ventrikelhypertrofi |
1.2.2 Øvrige undersøgelser
- Objektiv undersøgelse: særligt stetoskopi af hjerte og lunger.
- Biomarkører: Troponin tages ved ankomst til hospitalet og som udgangspunkt efter 1, 2 eller 3 timer afhængigt af lokal instruks og troponinassay. Diagnostisk og definitorisk for AMI anvendes 0 og 3 timers værdier, men 1 eller 2 timers målinger kan med fordel anvendes til tidlig stratificering. Liste over værdier ved brug af hhv. 0/1 og 0/2 time algoritmen er listet i Appendix 1.1. Hvis der fortsat er mistanke om AKS, og de første to prøver er negative, suppleres med yderligere prøve. Prøven analyseres som hastesvar (<1 time).
- Anden biokemi: hæmoglobin, trombocytter, INR, leukocyttal, CRP, natrium, kalium, kreatinin, blodsukker, HbA1c, total-, HDL- og LDL-kolesterol samt triglycerid.
- Ekkokardiografi: udføres akut hos hæmodynamisk ustabile patienter, ved kardial mislyd eller hvis der i øvrigt er mistanke om komplikationer til AKS. Desuden ved differentialdiagnostiske overvejelser som f.eks. lungeemboli, perikarditis og aortadissektion (se Appendix 1.2).
Ekkokardiografi skal foreligge forud for overflytning til subakut KAG.
- Rtg. af thorax og/eller fokuseret lungeultralyd kan udføres hos den inkompenserede patient og ved differentialdiagnostiske overvejelser.
1.3 Akut behandling
Hurtig diagnostik og behandling er afgørende for prognosen. Man skal ikke afvente svar på biomarkører før eventuel opstart af antitrombotika eller anden behandling, men basere den initiale behandling og triage på symptomer og EKG-forandringer.
Patienten konfereres akut med primær PCI center ved vedvarende smerter, akut hjertesvigt, kardiogent shock eller betydende arytmi.
Vedrørende vejledende retningslinjer for interhospital transport af patienter med AKS se Kapitel 2: Præ- og interhospital transport af hjertepatienter.
1.3.1 Invasiv undersøgelse og behandling ved AKS
Se Appendix 1.3 for timing af KAG.
STEMI
- ved symptomdebut <12 timer eller pågående symptomer indlægges/overflyttes patienten direkte til akut KAG på primær PCI center efter telemedicinsk visitation på baggrund af ambulance-EKG
- hvis ST-elevation først konstateres ved ankomst til lokalsygehus, arrangeres akut overflytning uden unødig forsinkelse
- Hvis der ikke foretages akut KAG, håndteres patienten som havende NSTEMI
NSTEMI/UAP
- ved ustabil hæmodynamik, livstruende arytmier eller vedvarende/recidiverende smerter anbefales akut KAG
- ved stabile patienter med en af følgende kliniske karakteristika tilstræbes KAG <24 timer
- NSTEMI med relevant klinik samt stigning og/eller fald i myokardiespecifikke biomarkører (se Appendix 1.1)
- dynamiske ST/T segment forandringer
- GRACE Risk Score >140
- hos patienter med UAP eller troponinforhøjelse, som ikke opfylder ovenstående kriterier, kan subakut hjerte CT anvendes. Ved mistanke om UAP hos patienter med lav a-priori risiko for koronar sygdom (fravær af ovenstående) anbefales primært non-invasiv iskæmi-udredning, som ofte kan foregå ambulant.
CABG
- se Afsnit 1.7
1.3.2 Akut antitrombotisk behandling ved STEMI
Antikoagulerende behandling
- ufraktioneret heparin (UFH) 7.500-10.000 i.e. i.v. præhospitalt eller ved overflytning til primær PCI
- såfremt patienten er i AK-behandling, konfereres med primær PCI center mhp. dosisreduktion eller undladelse af UFH
Trombocythæmmende behandling
- tabl. acetylsalicylsyre (ASA) 300mg tygges. Alternativt ASA 150-250 mg i.v.
- ADP-receptorblokker undlades som udgangspunkt inden KAG. Se Afsnit 1.3.4 og Afsnit 1.10.1
Fibrinolysebehandling
- alternativ til primær PCI - kan overvejes, hvis transporttiden til primær PCI center >2 timer
- kontraindikationer / praktisk udførelse, se Appendix 1.4
1.3.3 Akut antitrombotisk behandling ved NSTEMI / UAP
Antikoagulerende behandling
- fondaparinux 2,5 mg s.c. x 1 er 1.valg, lavmolekylært heparin (LMH) er 2. valg
- hvis eGFR <20 ml/min er fondaparinux kontraindiceret. I stedet anvendes LMH i halv dosis: inj. enoxaparin 1 mg/kg s.c. x 1 dgl. (max. 100mg x 1), eller dalteparin 120 i.e./kg x 1 s.c. (max. 10.000 i.e. x 1 s.c.)
- patienter i behandling med Vitamin K-antagonist (VKA) med INR >2,0 eller i behandling med Non-vitamin K antagonist Orale AntiKoagulantia (NOAK) kan fortsætte dette og skal ikke behandles med fondaparinux/LMH (se Afsnit 1.6.7)
Trombocythæmmende behandling
- tabl. acetylsalicylsyre (ASA) 300 mg
- ADP-receptorblokker undlades som udgangspunkt inden KAG. Se Afsnit 1.3.4 og Afsnit 1.10.1
1.3.4 ADP-receptorblokade
Som udgangspunkt gives ikke ADP- receptorblokker før KAG (for timing af KAG, se Afsnit 1.3.1 og Appendix 1.3), men i særlige tilfælde ved lang ventetid på KAG kan det overvejes evt. forudgået af konference med PCI center. For præparatvalg, dosis og behandlingsvarighed, henvises til Figur 1.2 og Afsnit 1.10.1.
Generelt:
- Hvis der skiftes fra én ADP-receptorblokker til en anden indenfor 30 dage efter AKS, anbefales almindeligvis ny loadingdosis.
- Behandlingsvarigheden af ADP-receptorblokker er som udgangspunkt 12 mdr., men kan individualiseres afhængigt af trombose- og blødningsrisiko. Se Afsnit 1.10.1
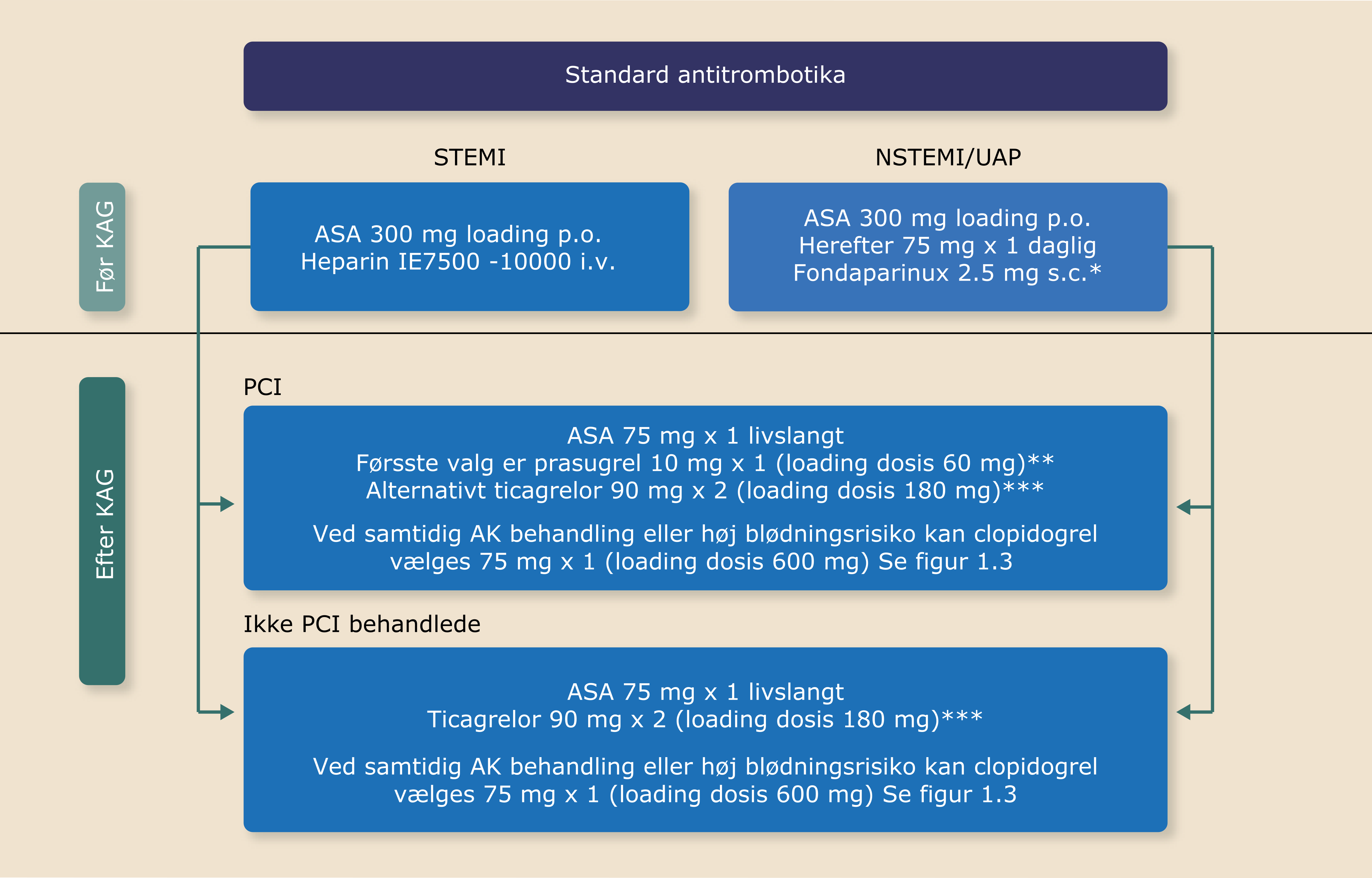 |
* hvis eGFR <20 ml/min anvendes LMH i halvdosis inj. enoxaparin 1 mg/kg s.c. x 1 dgl. (max. 100 mg x 1), eller dalteparin 120 i.e./kg x 1 s.c. (max. 10.000 i.e. x 1 s.c.) |
1.3.5 Understøttende / symptomatisk behandling ved AKS
Tabel 1.1: Understøttende / symptomatisk behandling ved AKS | |
Problem | Behandling |
|---|---|
Smerter |
|
Takyarytmi |
|
Bradykardi/blok |
|
Akut hjertesvigt |
|
Forhøjet blodtryk |
|
Kvalme |
|
Hypoksi |
|
1.4 Diagnostik når myokardiespecifikke biomarkører foreligger
Endelig diagnostik kan foretages, når der foreligger svar på serielle troponinmålinger (jf. lokale referenceintervaller for det anvendte troponinassay).
Tolkning:
Relevant klinik og
- ingen troponinværdier > 99-percentilen (uanset stigning og/eller fald) = UAP
- stabile troponinværdier > 99-percentilen = UAP hos patient med kronisk myokardiel skade eller differentialdiagnoser, se Appendix 1.2
- ≥1 troponinværdi over 99-percentilen, samt stigning og/eller fald = AMI (NSTEMI eller STEMI)
Kriterier for stigning og/eller fald, se Appendix 1.1.
1.5 Komplikationer til AKS
1.5.1 Arytmi
Arytmi inden for de første 24-48 timer kræver sjældent andet end symptomatisk behandling. Generelt anvendes betablokker og amiodaron til behandling af både ventrikulære og supraventrikulære takyarytmier forudsat, at patienten er hæmodynamisk stabil.
Hvis patienten er hæmodynamisk ustabil, skal der foretages akut DC-konvertering (se Tabel 1.2):
| Hæmodynamisk ustabil | Hæmodynamisk stabil |
|---|---|---|
Ventrikelflimren (VF) |
| |
Ventrikulær takykardi (VT) |
| |
Atrieflimren/atrieflagren |
|
|
Sinusbradykardi |
| |
AV-blok |
| |
1.5.2 Hjertesvigt
Hjertesvigt ved AMI er i de fleste tilfælde forårsaget af venstre ventrikelsvigt, men kan også skyldes mekaniske komplikationer som papillærmuskelruptur, ventrikelseptumdefekt eller myokardieruptur.
Stetoskopi og akut ekkokardiografi er altid indiceret ved AMI og kliniske tegn på akut hjertesvigt (f.eks. lungeødem). Ved kardiogent shock eller præ-shock konfereres med primær PCI center med henblik på overflytning, se i øvrigt Kapitel 4: Akut hjertesvigt
1.6 Særlige forhold ved AKS
1.6.1 Højresidigt infarkt
Ved isoleret højresidigt infarkt er det karakteristisk, at patienten er hypotensiv og fremtræder med halsvenestase, men uden tegn på lungestase.
EKG vil ofte vise ST-segment elevation i II, III og aVF, men elevationer ses også i de højresidige afledninger V3R-7R. Desuden kan såvel ST-segment elevation som depression ses i V1-V3.
Ekkokardiografi bør udføres akut ved mistanke om højresidigt infarkt for at få information om højre ventrikels størrelse og funktion.
Den akutte behandling, ud over PCI, er infusion af væske under tæt monitorering grundet risiko for lungeødem, hvis venstre ventrikel er medinvolveret. Desuden infusion af dopamin for at opretholde et adækvat blodtryk og øge minutvolumen. Evt. atropin 0,5-1 mg i.v. eller transvenøs pacing ved bradykardi.
Undgå preload reducerende farmaka som diuretika og nitroglycerin. Se Kapitel 4: Akut hjertesvigt, Afsnit 4.5.4.
1.6.2 Type 2 infarkt
Type 2 infarkt er per definition ikke udløst af en koronar trombe, men sekundært til øget krav eller nedsat tilførsel af oxygen, Se Appendix 1.1.
Behandlingen rettes mod den udløsende årsag. Antitrombotisk og invasiv udredning/behandling skal individualiseres og bør konfereres med kardiologisk speciallæge.
1.6.2.1 Spontan koronar dissektion
Spontan koronardissektion (SCAD) er en blødning i koronarkarvæggen, som kompromitterer koronarflowet. Klinikken varierer fra svær påvirkning med kraftige smerter, arytmier, akut hjertesvigt til kortvarigt brystubehag. Behandlingen besluttes individuelt (medicinsk behandling, PCI eller CABG). Hos stabile patienter med bevaret koronar flow vil behandlingen oftest være medicinsk. Som udgangspunkt anbefales ASA og clopidogrel i op til 12 mdr. til patienter, som PCI behandles, men kan også overvejes, hvis patienten ikke er invasivt behandlet og er uden øget blødningsrisiko.
Der anbefales observation til smertefrihed med fokus på blodtrykskontrol og antianginøs behandling. Betablokker kan muligvis reducere recidivrisikoen. Forløbet kan være mere langvarigt end det vanlige AKS forløb.
Der anbefales vanlig rehabilitering, dog frarådes motion de første tre måneder og kraftig isometrisk belastning (livslangt).
1.6.2.2 Myokardieinfarkt uden obstruktiv koronarsygdom (MINOCA)
AMI uden obstruktiv koronarsygdom (MINOCA) er til stede, når følgende kriterier er opfyldt:
- AMI diagnosen er sikker (jf. Afsnit 1.1)
- KAG uden betydende stenoser
- ingen anden oplagt klinisk årsag der kan forklare den akutte præsentation
MINOCA skal betragtes som en arbejdsdiagnose, indtil nærmere diagnostik er foretaget. Diagnostiske forslag: udredning med provokationstest til afklaring af spasme (foretages under KAG), udredning for mikrovaskulær sygdom (CFR måling under KAG eller ved PET scanning), intrakoronar billeddannelse til visualisering af evt. plaque ruptur/trombe, udelukkelse af SCAD. MR- eller CT-scanning med henblik på udelukkelse/verificering af koronar aterosklerose og regionale infarktforandringer. Differentialdiagnoser som lungeemboli, takotsubo m.v. kan også overvejes.
Dobbelt blodpladehæmning kan overvejes, men afhænger af den formodede underliggende ætiologi, og evidensen er sparsom. Ved mistanke om takotsubo kardiomyopati overvejes afhængigt af blødningsrisiko at fortsætte ASA og ADP- receptorblokker i doser som ved AKS, indtil diagnosen er endeligt verificeret eksempelvis ved normalisering af LVEF eller fravær af tegn på infarkt på MR- skanning.
Behandling med statin, ACE hæmmer, calciumantagonist og betablokker kan overvejes afhængigt af den formodede underliggende ætiologi.
Der anbefales vanlig rehabilitering.
1.6.3 Diabetes mellitus
AKS patienter med diabetes mellitus type 1 og 2 har væsentligt øget mortalitet.
Ved invasiv undersøgelse med anvendelse af røntgenkontrast kan metformin fortsættes, hvis nyrefunktionen er normal.
Ved nedsat nyrefunktion (eGFR <60 ml/min) anbefales det om muligt at pausere metformin 48 timer før invasiv undersøgelse. Metformin kan genoptages 48 timer efter proceduren, hvis nyrefunktionen ikke er forringet.
1.6.4 Nyreinsufficiens
Alle ældre (>75 år) og patienter med lav kropsvægt (<60 kg) kræver særlig opmærksomhed, idet nær-normal S-kreatinin kan være associeret til en lavere kreatininclearance end forventet.
Nyrefunktionen bør vurderes ved eGFR, og hvis nyrefunktionen er nedsat, skal det overvejes at reducere dosis eller evt. helt undgå en række farmaka, f.eks. enoxaparin, dalteparin, fondaparinux, bivalirudin, atenolol, ACE-hæmmere, angiotensin-II antagonister og NOAKs.
Forebyggelse af kontrastnefropati:
Risikoen for kontrastnefropati ved KAG kan reduceres ved at sikre, at patienten er velhydreret, holde pause med nefrotoksiske stoffer og begrænse kontrastforbruget.
Se Kapitel 35: Farmaka og kardiovaskulære symptomer, Afsnit 35.2.4.
1.6.5 Anæmi
Hæmoglobin ved indlæggelsen er en uafhængig prognostisk markør for risikoen for iskæmiske hændelser samt blødningskomplikationer inden for 30 dage. Medmindre der er tale om anæmibetinget type 2 infarkt, bør blodtransfusioner generelt ikke gives til hæmodynamisk stabile patienter uden pågående iskæmi med hæmatokrit >25% eller hæmoglobin >4,5 mmol/l.
1.6.6 Ældre
Som udgangspunkt bør ældre tilbydes samme diagnostiske og terapeutiske strategier som yngre patienter dog med fokus på nytte-risiko ratio, komorbiditet og patientpræferencer.
Den antitrombotiske behandling skal principielt følge samme retningslinjer som hos yngre patienter, men med speciel hensyntagen til den generelt øgede blødningsrisiko hos ældre (jf. ovenfor).
1.6.7 Patienter i peroral antikoagulansbehandling
Generelt:
Flerstofsbehandling med NOAK/VKA, ASA og ADP-receptorblokker (dual og triple terapi) medfører betydelig øget blødningstendens. Indikationen skal altid vurderes individuelt på baggrund af koronartrombose-, tromboemboli- og blødningsrisiko. Varigheden af triple terapi bør begrænses mest muligt jf. Figur 1.3, og så vidt muligt undgås til fordel for dual terapi med NOAK/VKA og clopidogrel. Figuren viser den maksimalt anbefalede varighed af triple terapi.
Varighed af behandling med ASA og ADP-receptorblokker bør fastlægges af PCI-operatør efter proceduren.
Alle patienter loades med ASA, der normalt fortsættes i op til 7 dage, og almindeligvis seponeres ved udskrivelse.
Normalt anbefales clopidogrel som ADP-receptorblokker. Ticagrelor og prasugrel anvendes kun hos særligt udvalgte patienter.
Ved non-valvulær atrieflimren eller venøs tromboembolisk sygdom anbefales NOAK frem for VKA.
Ved opstart af dual terapi med ADP-receptorblokker og NOAK anbefales apixaban, rivaroxaban eller dabigatran p.g.a. bedst dokumentation for sikkerheden. Hos patienter med øget risiko for GI blødning, foretrækkes apixaban.
Protonpumpehæmmer behandling skal gives profylaktisk ved tripleterapi og bør overvejes ved kombinationsbehandling med ADP-receptorblokker og NOAK/Marevan (se Afsnit 1.6.9).
Dosering af NOAK ved samtidig trombocythæmning:
- apixaban 5 mg x 2 dagligt
- dabigatran 150 mg x 2 dagligt, men overvejes reduceret til 110 mg x 2 dagligt ved høj blødningsrisiko og/eller høj alder
- rivaroxaban 20 mg x 1 dagligt, men bør overvejes reduceret til 15 mg x 1 dagligt ved høj blødningsrisiko og/eller høj alder.
- edoxaban 60 mg x 1 dagligt
I øvrigt skal kriterierne for generel dosisreduktion (nedsat nyrefunktion, alder, vægt <60 kg eller medicininteraktioner) følges. Se Kapitel 14: Peroral antikoagulansbehandling, Afsnit 14.4.2.
Dosering af VKA ved samtidig trombocythæmning:
Der anbefales stram styring af INR lavt i terapeutisk niveau (2,0-2,5), så længe behandlingen kombineres med ASA og/eller ADP-receptorblokker undtaget ved mekanisk mitralklapprotese og mitralstenose med AFLI, hvor INR skal være mellem 2,5 og 3,5.
Figur 1.3: Vejledende anbefaling til AKS patienter i AK behandlig |
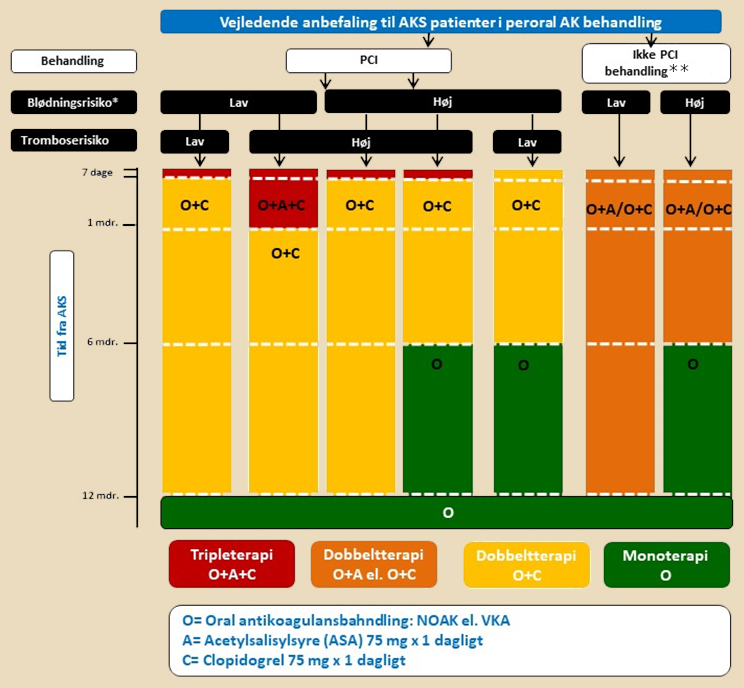 |
*Til vurdering af blødnings- og tromboserisiko se afsnit 1.10 |
1.6.8 Non-steroide anti-inflammatoriske lægemidler (NSAID)
NSAID skal så vidt muligt undgås ved iskæmisk hjertesygdom, specielt ved samtidig hjertesvigt.
NSAID kan hæmme effekten af ASA og bør derfor gives minimum 2 timer efter ASA indtagelse.
Se i øvrigt Kapitel 35, Afsnit 35.1: Farmaka og kardiovaskulære komplikationer
1.6.9 Protonpumpe hæmmer (PPI) behandling
Profylaktisk PPI behandling (pantoprazol 40 mg x 1 er førstevalg) bør overvejes til patienter i behandling for AKS ved følgende:
- AK behandling kombineret med ASA og/eller ADP receptorblokker
- alder ≥65 år
- tidligere øvre gastrointestinal blødning/ulcus
- dyspepsi / gastrointestinal refluks
- helicobactor pylori infektion
- kronisk alkoholoverforbrug
- vedvarende behov for NSAID/steroid behandling
1.7 Koronar by-pass operation (CABG) ved AKS
CABG-tidspunkt fastlægges af hjerteteam ud fra en individuel vurdering af optimalt operationstidspunkt.
Plan for antitrombotisk behandling op til CABG lægges af hjerteteam. Som hovedregel behandles med LMH indtil aftenen før operationen, alternativt med fondaparinux indtil 36 timer før operationen. Som hovedregel holdes pause med clopidogrel 5 dage før, ticagrelor 3-5 dage før, og prasugrel 7 dage før CABG, mens ASA ikke pauseres forud for operation. ADP-receptorblokker behandling er kun en relativ kontraindikation for akut CABG-operation.
Pausering af peroral AK behandling følger anbefalingerne i Kapitel 14.
Den antitrombotiske behandling med ASA og ADP-receptorblokker skal genoptages efter CABG (ticagrelor er førstevalg) og fortsættes vanligvis i 12 mdr., herefter monoterapi i.h.t. ovenstående retningslinjer.
Patienter, der får foretaget coronar bypass operation og har samtidig indikation for AK behandling bør behandles med hjertemagnyl og marevan/NOAK. Såfremt patienten vurderes til at være i øget blødningsrisiko (se afsnit 1.10), kan trombocythæmmer (magnyl) behandlingen seponeres. Dog anbefales dette tidligst efter 6 mdr. (medmindre der ses blødningskomplikationer).
1.8 Anden kirurgi
ADP-receptorblokker behandling bør pga. risiko for stenttrombose ikke pauseres inden for 3 mdr. efter implantation af stent uden grundig individuel vurdering, ofte i samråd med PCI-center. Se Kapitel 24.
Der er normalt ikke indikation for pausering af ASA.
1.9 Indlæggelses- og EKG-monitoreringsvarighed
Indlæggelse – og telemetrivarighed baseres generelt på den kliniske tilstand samt på individuelle behov for information og rehabilitering.
Ved STEMI anbefales mindst 24 timers monitorering og 48 timers indlæggelse hos lavrisikopatienter (<70 år, LVEF>45%, 1-2 karssygdom, fuld revaskularisering, rytmestabil).
Ved NSTEMI/UAP anbefales monitorering indtil patienten er revaskulariseret. Indlæggelsesvarighed efter revaskularisering efter individuel vurdering.
1.10 Efterbehandling
1.10.1 Antitrombotisk behandling
Efterbehandling (præparatkombination og behandlingsvarighed) med ASA, ADP-receptorblokker og evt. perorale antikoagulantia bør fastsættes af det invasive center under hensyntagen til patientens trombose- og blødningsrisiko, PCI-behandlingens kompleksitet og den anvendte stenttype.
ASA: Tabl. ASA 75 mg x 1 livslangt. Ved ASA-intolerans gives ticagrelor eller prasugrel efter gældende retningslinjer op til 12 mdr. og herefter clopidogrel livslangt.
ADP-receptorblokker: Generelt anbefales ADP-receptorblokker i 12 mdr., men behandlingsvarigheden kan i samråd med PCI-center afkortes eller forlænges (se nedenfor). Valg af ADP-receptorblokker afhænger af patientens blødningsrisiko, og om der er foretaget PCI.
Efter PCI:
- Førstevalg er tabl. prasugrel. Dosering: 60 mg loading dosis, herefter 10 mg x 1 dgl. i 12 mdr. (5 mg x 1 ved alder >75 år eller vægt <60 kg). Prasugrel er kontraindiceret ved tidligere apopleksi/TIA.
- Alternativt kan gives tabl. ticagrelor. Dosering: 180 mg loading dosis, herefter 90 mg x 2 dgl. i 12 mdr. Ticagrelor er kontraindiceret ved tidligere intrakraniel blødning.
- Ved samtidig behandling med NOAK eller VKA, eller hvis patienten har øget blødningsrisiko, vælges tbl. clopidogrel. Dosering: 600 mg loading dosis, herefter 75 mg x 1 dgl. i op til 12 mdr.
Patienter, der ikke får foretaget PCI:
- Førstevalg er ticagrelor. Dosering som angivet ovenfor.
- Ved samtidig behandling med NOAK eller VKA, eller hvis patienten har øget blødningsrisiko, vælges clopidogrel. Dosering som angivet ovenfor.
Blødningsrisiko: kan bl.a. vurderes ved risikoscores som PRECISE-DAPT, Crusade bleeding score og ARC-HBR (med iOS eller Android). Se Kapitel 15: Atrieflimren og atrieflagren, Tabel 15.4.
Ved høj risiko, som f.eks PRECISE-DAPT score ≥25, kan ADP-receptorblokker behandlingsvarighed afkortes til 1-6 mdr.
Tromboserisiko: Anses for høj ved følgende risikofaktorer
- tidligere myokardieinfarkt
- diabetes
- kompleks koronaranatomi som flerkarssygdom eller stentning af hovedstamme eller bifurkatur
- perifer arteriel sygdom
- eGFR <60 ml/min
- Tidligere stenttrombose
Hvis en eller flere af disse risikofaktorer er til stede, og der de første 12 mdr. ikke har været blødningskomplikationer, kan ADP-receptorblokker behandlingen overvejes forlænget med ticagrelor i nedsat dosering 60 mg x 2 dgl. op til 36 måneder.
Det skal tilstræbes, at det invasive center vurderer, om patienten kan være kandidat til forlænget behandling, men hvis der ikke er taget stilling til dette under den primære indlæggelse, bør det gøres inden afslutning af rehabiliteringsforløbet. Endelig beslutning kan dog først tages, når planlagt behandling er gennemført uden blødningskomplikationer.
Lavdosis NOAK:
Lav dosis NOAK kan overvejes hos udvalgte patienter:
- når ASA plus ADP-receptorblokker ikke kan anvendes
- efter endt dobbelt blodpladehæmmerbehandling, hvor den individuelle risiko for trombose vurderes høj og blødningsrisikoen lav, OG følgende kriterier er opfyldt:
- aterosklerose i mindst 2 vaskulære gebeter (koronar, cerebrovaskulært, perifer arteriel sygdom), eller
- alder ≥65 år, eller
- alder <65 år med samtidig minimum to risikofaktorer: rygning, diabetes, eGFR <60 (men eGFR>15), hjertesvigt (LVEF <30%), non-hæmoragisk apopleksi ≤1 md.
Behandlingsvalg: Tabl. rivaroxaban 2,5 mg x 2 dagligt i kombination med ASA. Evt. fortsat behandlingsindikation revurderes efter 12 mdr. Forsigtighed ved alder >75 år, legemsvægt <60 kg og høj blødningsrisiko.
1.10.2 Anden medicinsk behandling
Højdosis statinbehandling med atorvastatin 80 mg x 1 eller rosuvastatin 40 mg x 1 dgl. opstartes under indlæggelsen og anbefales livslangt. Hvis det allerede under indlæggelsen står klart, at behandlingsmålet ikke nås ved statin alene, overvejes at tillæge ezetimibe 10 mg x 1 dgl. Kontrol efter 1-2 mdr. med tillæg af ezetimibe til statin, hvis behandlingsmålet ikke er nået. Se Kapitel 28: Dyslipidæmi, Afsnit 28.1 for behandlingsmål.
Betablokkerbehandling kan anvendes til patienter uden hjertesvigt i op til 2 år efter STEMI (fx metoprolol i depotformulering med startdosis 50 mg x 1). Patienter med systolisk hjertesvigt behandles i henhold til gældende retningslinjer. Se Kapitel 5: Kronisk hjertesvigt.
ACE-hæmmerbehandling er indiceret til alle patienter med klinisk hjertesvigt eller LVEF ≤40% efter overstået akut fase (inkl. evt. revaskularisering) med videre ambulant optitrering i hjertesvigtsklinik. Anbefales desuden til alle patienter med diabetes, hypertension, kronisk nyresygdom, perifer arteriel sygdom eller i øvrigt høj risiko for efterfølgende iskæmiske hændelser. Ved intolerans anvendes angiotensin-II-receptorblokker.
Aldosteronantagonistbehandling anbefales hos patienter med inkompensation eller LVEF <40% ≤14 dage efter AMI. For specifikke doser og optitreringsforslag se Kapitel 5: Kronisk hjertesvigt, Afsnit 5.5.1.
Venstre ventrikeltromber (muraltromber) behandles som udgangspunkt med VKA og LMH. LMH gives i min. 5 dage, og indtil INR har været i niveau i 2 døgn. NOAK har også været anvendt med gode resultater. Der anbefales min. 3 mdrs. behandling med fornyet ekkokardiografi inden seponering af antikoagulerende behandling. Anteriort STEMI med apikal akinesi uden påvist trombe indicerer ikke profylaktisk AK-behandling. Se Kapitel 25: Kardiel embolikilde og Kapitel 14: Antikoagulationsbehandling.
1.10.3 Rehabilitering
Alle patienter med AKS, uanset om der er foretaget revaskularisering, skal tilbydes et integreret rehabiliteringsforløb med fokus på tobaksophør, kolesterolsænkende behandling, optimering af hypertensions- og diabetesbehandling, kostvejledning/evt. vægtreduktion samt fysisk træning, se Kapitel 29: Hjerterehabilitering.
Herudover skal følgende forhold iagttages:
- sygemelding – individualiseres, sædvanligvis 1-4 uger
- bilkørsel – Se Kapitel 38: Kørekort hos patienter med hjertelidelser
- rejser – før udlandsrejser indenfor første halve år anbefales kontakt til rejseforsikringsselskab
- forsikringsanmeldelse overvejes (”Kritisk sygdom”)
- henvisning til udredning ved klinisk mistanke om familiær hyperkolesterolæmi. (se Kapitel 32: Arvelige hjertesygdomme og Kapitel 28: Dyslipidæmi)
1.10.4 Ekkokardiografi
Alle patienter med AKS bør inden udskrivelse have foretaget ekkokardiografi.
1.10.5 Profylaktisk ICD
Primær profylaktisk implantation af ICD overvejes ved nedsat LVEF ≤35 % samt NYHA klasse II eller III trods optimal medicinsk behandling. Som hovedregel vurderes LVEF tre måneder efter AMI før endelig stillingtagen til ICD implantation.
Vedrørende anvendelse af ICD/CRT pacemaker og ICD, se Kapitel 19: Pacemakerbehandling og Kapitel 20: Implanterbar defibrillator (ICD)
1.11 Influenzavaccination
Det anbefales, at patienter med AMI, der opstår under influenzasæsonen (1. oktober til 1. marts), under indlæggelsen tilbydes vaccination for influenza, såfremt de ikke allerede er vaccineret i indeværende sæson. Der anbefales desuden efterfølgende årlig influenzavaccination til alle med tidligere AKS.






