18. Ventrikulær takykardi
18.1 Definition
Ventrikulær arytmi udgår fra strukturer distalt for His’ bundt i venstre eller højre ventrikel uafhængigt af atrier eller AV-knuden.
18.2 Inddeling
Ventrikulær arytmi inddeles som nedenfor anført:
- subtype:
- præmatur ventrikulær kompleks (PVC): præmaturt og abnormt udseende kompleks med QRS varighed ≥120 ms uden forudgående P-tak
- ventrikulær takykardi (VT): ≥3 konsekutive komplekser med frekvens >100 udgående fra ventriklerne, uafhængig af aktivitet i atrier og AV-knuden.
- udseende:
- PVC: ensartet (monofokalt) eller forskelligartet udseende (multifokalt)
- ventrikulær takykardi:
- monomorf: ensartet QRS-mønster
- polymorf: vekslende QRS-mønster fra kompleks til kompleks
- torsades de pointes: subtype af polymorf VT med forudgående forlænget QT-interval med vedvarende skiftende QRS-akse i et sinusoidalt mønster
- ventrikelflimren: uorganiseret elektrisk aktivitet med hurtige og bizarre komplekser, der veksler konstant i frekvens og størrelse uden sikkert identificerbare QRS-komplekser
- varighed:
- non-sustained VT: <30 sek. varighed
- sustained VT: ≥30 sek. varighed eller afbrudt inden da af DC-stød eller implanterbar cardioverter defibrillator (ICD) terapi
- incessant VT: sustained VT som persisterer i flere timer
- hyppighed:
- elektrisk storm: ≥3 episoder med VT/VF indenfor 24 timer og ≥5 minutter imellem hver VT/VF-episode, som kræver enten ATP eller kardiovertering/defibrillering
18.3 Ætiologi
Ventrikulær arytmi optræder:
- som ledsagefænomen til en række strukturelle hjertesygdomme:
- koronararteriesygdom (akut/kronisk iskæmi og koronaranomali)
- kardiomyopati (dilateret, arytmogen, opereret kongenit hjertesygdom og neuromuskulær)
- klapsygdom
- myokardit/sarkoidose/infiltrativ sygdom
- ved sygdomme med strukturelt normalt hjerte:
- idiopatisk ventrikulær udløbsdelstakykardi
- idiopatisk venstre ventrikel-takykardi
- ionkanalsygdomme (langt og kort QT-syndrom, Brugada syndrom, katekolaminerg polymorf ventrikulær takykardi, tidlig repolariseringssyndrom)
- som proarytmi udløst af:
- antiarytmisk behandling
- lægemidler, som forlænger QT intervallet (fx psykofarmaka)
- ved elektrolytforstyrrelser:
- særlig s-kalium (K+)
18.4 Udredning
18.4.1 Udredningsprogram
Den kliniske manifestation af ventrikulær arytmi er mangeartet og udredningen vejledes af anamnese og klinisk mistanke om udløsende årsag jf. Tabel 18.1. Anamnese med uvarslet synkope, velkendt arvæv i myokardiet og familiær historie med tidlig hjertedød samt specifikke EKG-karakteristika (Afsnit 18.4.3 EKG) øger risikoen for ventrikulær arytmi.
Hyppige manifestationer af ventrikulær arytmier andrager :
1) tilfældigt opdaget hyppig PVC eller non-sustained VT på Holter/telemetri
2) sustained monomorf VT
3) patienter, der overlever hjertestop
4) pludselig hjertedød
5) familieudredning af pårørende til patienter, der enten har overlevet eller døde af hjertestop. Nedenstående skema kan vejlede udredning af ventrikulær arytmi.
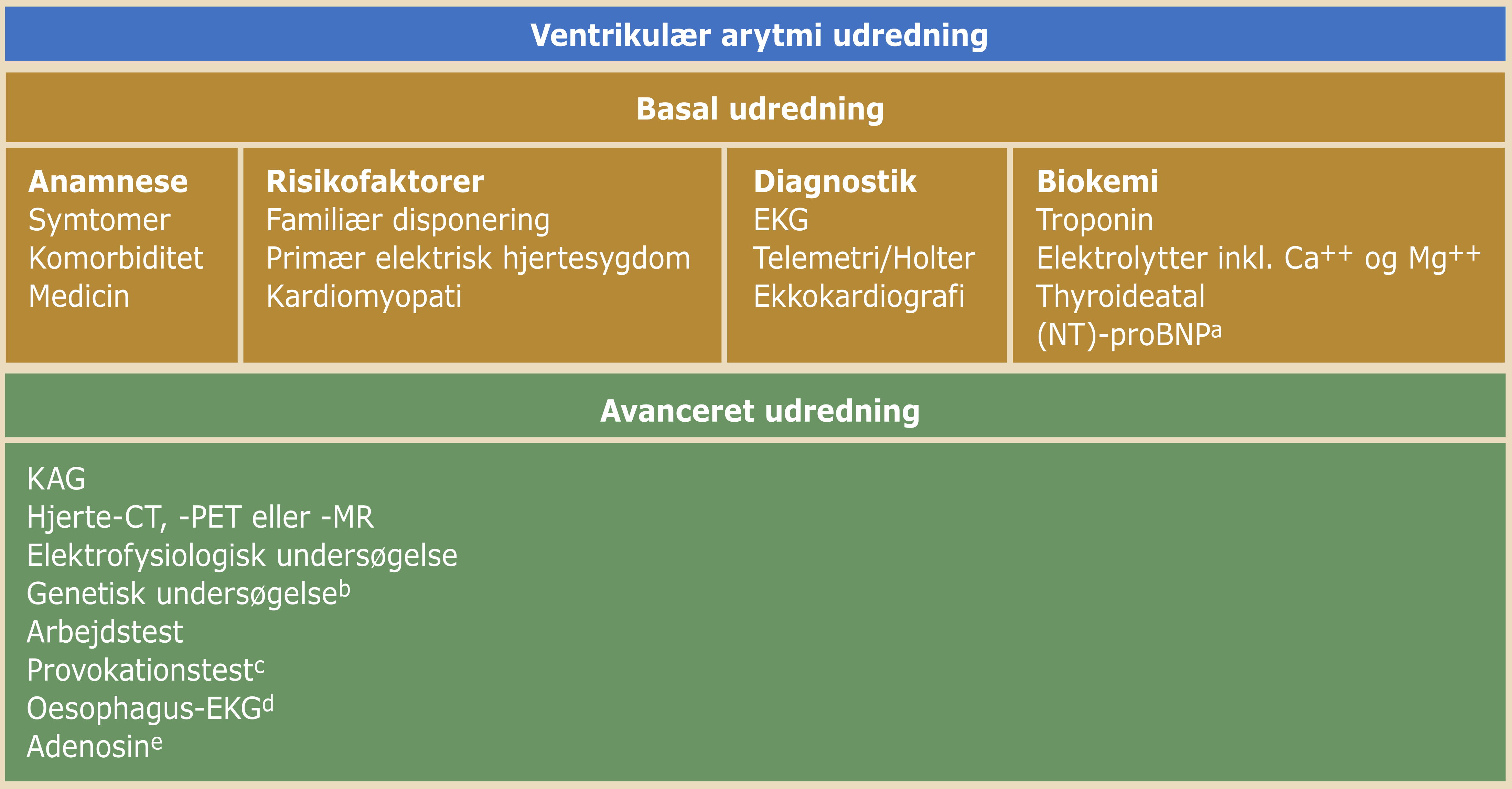 |
aIkke nødvendigt, hvis ekko er nemt tilgængeligt. bKun efter aftale med klinik for arvelige hjertesygdomme. cFx ajmalintest ved Brugadas syndrom. dKun hos stabile patienter, hvor P-QRS relationen ønskes afklaret under takykardi. eKun i enkeltstående tilfælde med diagnostisk uklarhed. 6-18mg i.v., hvis der er regelmæssig breddeøget takykardi med typisk grenbloksmønster. Ovenstående er vejledende forslag til udredning og kun selekterede undersøgelser bør udføres. |
18.4.2 Diagnostiske overvejelser
Ved breddeøget takykardi er der nedenstående diagnostiske muligheder. Hvis der fortsat er usikkerhed om arytmitypen, kan elektrofysiologisk undersøgelse overvejes senere i forløbet.
- VT
- SVT med temporært/permanent grenblok (RBBB eller LBBB), intraventrikulær conduction delay (IVCD) eller præexcitation (WPW), og pacemaker-medieret takykardi (PMT)
- artefakt (muskelkontraktioner, elektrisk støj, løs elektrode etc.)
18.4.3 EKG
Enhver breddeøget takykardi skal som udgangspunkt opfattes som ventrikulær. Diskrimination mellem SVT med aberration og VT kan være udfordrende. Der findes flere simple og avancerede EKG algoritmer, som kombinerer flere kriterier for at øge den diagnostiske evne (se speciallitteratur). Ved tvivl om diagnosen taler følgende tegn for VT (listen er ikke udtømmende):
- QRS-bredde:
- ≥160ms
- QRS-konfiguration:
- V1: R-tak eller Rr'-mønster
- V1/V2: R-tak >30ms
- V1/V2: RS-interval >60ms
- V1/V2: uregelmæssig "notched" nedadgående del af S-tak
- V6: Q-tak, QS-mønster eller rS-mønster
- V1-V6: udelukkende positiv eller negativ QRS-konkordans
- ukarakteristisk RBBB eller LBBB morfologi
- QRS-akse:
- akseskift sammenholdt med QRS-aksen i sinusrytme
- AV/VA-overledning:
- AV-dissociation
- retrograd atrial aktivering med intermitterende VA-blok (flere QRS end retrograde p-takker)
- intermitterende "capture beats" eller "fusion beats"
- Øvrige:
- PVC under sinusrytme med fuld kompensatorisk pause med samme QRS-konfiguration som under den breddeøgede takykardi
- hos udvalgte stabile patienter kan P-QRS relationen evt. undersøges under takykardien med oesofagus-EKG
18.5 Behandling
18.5.1 Generel behandling
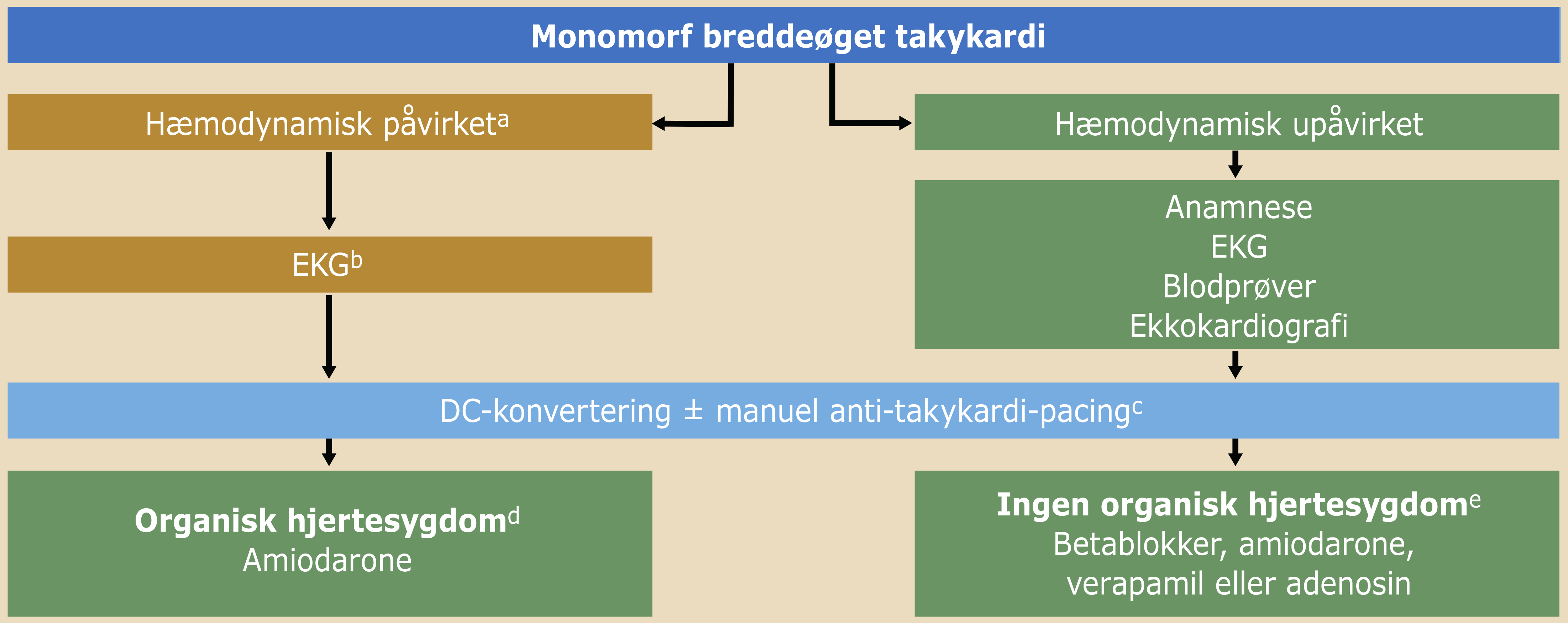
Udredning og behandling af monomorf breddeøget takykardi
Nedadstående figur viser skematiske forslag til udredning og behandling af monomorf breddeøget takykardi
Udredning og behandling af polymorf breddeøget takykardi
Nedadstående figur viser skematiske forslag til udredning og behandling af polymorf breddeøget takykardi
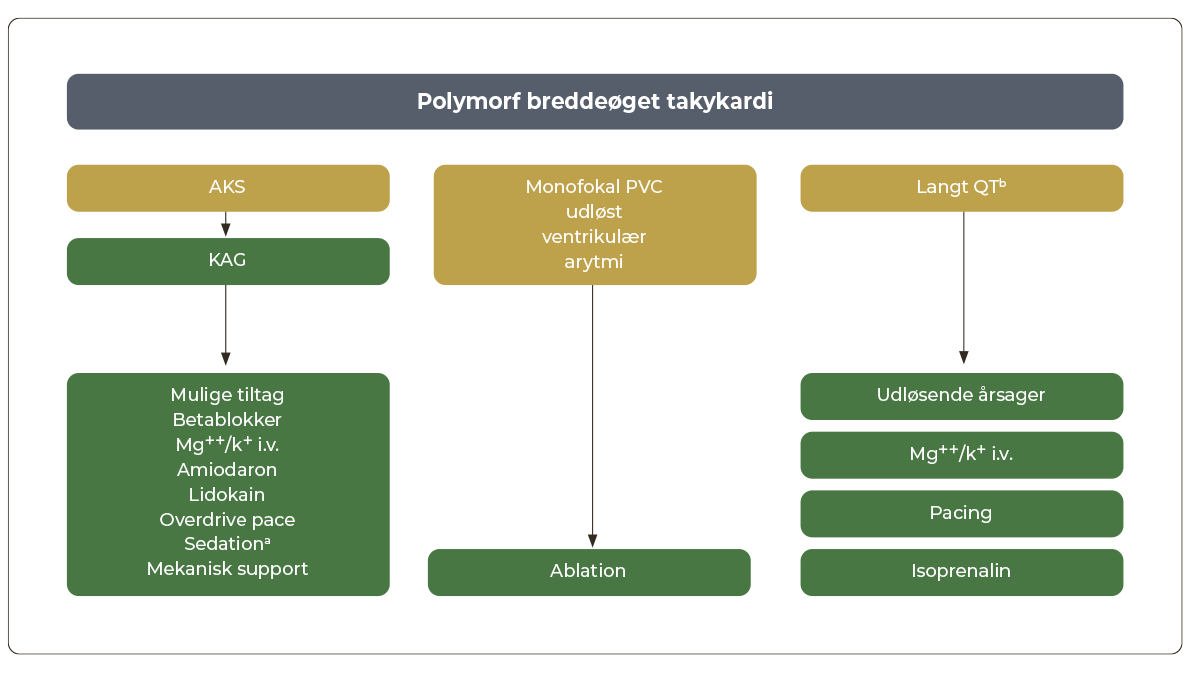 |
aSedation er indiceret hos hæmodynamisk stabile patienter (patientlindrende) eller når der er recidiverende ventrikulær arytmi trods medicinsk behandling. bBetablokker er førstevalget ved arveligt langt QT syndrom, hvor isoprenalin ikke tilrådes. |
Hæmodynamisk påvirket patient er karakteriseret ved (4s):
- shock; herunder systolisk blodtryk <90mmHg, tegn på hypoperfusion og/eller
- synkope: påvirket/tab af bevidsthedsniveau og/eller
- svigt: venstresidig hjertesvigt med dyspnø/lungeødem og/eller
- smerter: angina pectoris
Disse patienter skal behandles akut med synkroniseret DC-konvertering med maksimal energi (alt efter defibrillatormodel) fra første stød i sedation eller generel anæstesi.
Elektrisk storm/incessant VT hos patienter med og uden ICD:
Patienter med elektrisk storm skal indlægges, da situationen er livstruende. Akut behandling og interrogation af ICD-enheden er nødvendig. Utilsigtet ICD-terapi skal udelukkes eller forsøges behandlet. Hvis ICD-programmer ikke er tilgængeligt, kan ICD-terapier inhiberes ved at lægge en magnet over ICD-enheden.
Der må ofte foretages flere foranstaltninger samtidigt. HSE bør kontaktes tidligt i forløbet mhp. akut behandling, udredning og ofte overflytning. Foranstaltninger i den akutte fase fremgår af Figur 18.1 og Figur 18.2.
Hæmodynamisk upåvirket patient:
Synkroniseret DC-konvertering skal indtænkes meget tidligt i behandlingen, og i ventetiden frem til synkroniseret DC-konvertering bør medicinsk behandling initieres iht. Figur 18.1 og Figur 18.2. ICD-patienter kan forsøges behandlet med manuel anti-takykardi-pacing (ATP) via ICD-programmer. Dette skal foregå under hjertestopberedskab med pads påsat anterolateralt (ICD i venstre side) eller anteroposteriort (ICD i højre side) koblet til tændt defibrillator, sedativa og samtidig mulighed for respirationstøtte/anæstesi-assistance.
Subakut KAG bør foretages hos patienter med polymorf VT/VF. Polymorf VT ved akut koronart syndrom behandles herudover med betablokker og ved behov amiodaron. Lidokain kan tillægges, hvis betablokker og amiodaron har utilstrækkelig rytmestabiliserende effekt.
Medicinsk behandling:
Nedenstående er anført dosering og forholdsregler ved de hyppigst anvendte farmaka ved ventrikulær arytmi jf. Figur 18.1 og Figur 18.2:
- Amiodaron 150-300mg i.v. over 20-30min. efterfulgt af kontinuerlig infusion (900mg over 24t). Blodtryk skal monitoreres tæt grundet risiko for blodtryksfald. Bolus kan administreres i velfungerende i.v. adgang anlagt i cubital vene, kontinuerlig infusion skal administreres i centralt anlagt vene kateter.
- Metoprolol 2,5-5mg i.v. over 5min. Stor forsigtighed ved lav LVEF pga. negativ inotrop effekt. Ydermere forefindes metoprolol i.v. ikke på alle hospitaler.
- Lidokain kan gives ved manglende effekt af amiodaron og betablokker hos patienter med akut koronart syndrom og til patienter med strukturel hjertesygdom og monomorf VT. Lidokain bolus 1-2mg/kg legemsvægt i.v. efterfulgt af kontinuerlig infusion 1-4mg/min kan administreres i perifer i.v. adgang. Hvis virkning ikke ses efter første injektion, kan yderligere gives én eller to injektioner med 5-10min. interval. Der skal ydes særlig opmærksomhed om, at bolus lidokain doseres efter kropsvægt (mg/kg), mens kontinuerlig infusion doseres i mg/min. Behandlingen fortsættes sædvanligvis med kontinuerlig i.v. infusion under konstant overvågning. Kontinuerlig lidokain infusion må kun anvendes i få dage.
Hvis ovenstående behandling har utilstrækkelig rytmestabiliserende effekt, kan én eller flere af nedenstående behandlinger tillægges efter konference med HSE:
- Isoprenalin 0,05-0,2μg/kg/min til QRS-frekvens 80-100/min ved erhvervet langt QT-syndrom med tilbagevendende torsades de pointes VT trods optimering af udløsende faktorer og magnesium
- Magnesium og/eller kalium infusion iht. lokale retningslinjer indtil Mg++>0,80 mmol/l og K+ >4,0mmol/l
- Generel anæstesi: propofol kan reducere arytmi tilbøjeligheden ved at mindske sympatisk stress-respons. Denne mulighed skal tidligt tænkes ind i behandlingen.
Non-medicinsk behandling:
- Ablation: ved behandlingsrefraktær monomorf VT skal HSE kontaktes mhp. subakut radiofrekvensablation. Ablation er effektiv hos patienter med tidligere myokardieinfarkt, og kan også være effektiv hos patienter med non-iskæmisk kardiomyopati og VF udløst af kortkoblet PVC.
- Ekstrakorporal cirkulationsstøtte: overvejes ved behandlingsrefraktær hæmodynamisk betydende VT og recidiverende VF. Behandlingen foregår på HSE.
- Genetisk udredning: kan foretages ved sandsynlig arvelig årsag. Sygdomme, der bør tilbydes familieudredning, fremgår af Kapitel 32: Arvelige hjertesygdomme, Afsnit 32.2.
- ICD-enhed: oftest er baserate øgning til 80-100 per min tilstrækkelig til at supprimere PVC og afkorte QT og dermed nedsætte risiko for recidiverende ventrikulær arytmi. For yderligere information vedrørende indikation og potentielle ICD komplikationer henvises til Kapitel 20: Implanterbar cardioverter defibrillator (ICD), Afsnit 20.2 og Afsnit 20.4.
18.5.2 Ætiologibestemt udredning og behandling
Sustained VT hos patienter med og uden påviselig strukturel hjertesygdom: udredning og behandling følger allerede skitserede tiltag under Tabel 18.1, Figur 18.1 og Figur 18.2. Behandlingsvalget – fx ICD og ablation – vurderes på HSE. I vurderingen indgår patientens præference, alder, underliggende hjertesygdom og antal VT-morfologier. Hjertesvigt følger vanlige retningslinjer, som anført i Kapitel 5: Kronisk hjertesvigt.
Non-sustained VT hos patienter med tidligere myokardieinfarkt: elektrofysiologisk ekspertise på HSE bør rådføres mhp. yderligere udredning og evt. implantation af profylaktisk ICD – særligt i de tilfælde, hvor der er uforklaret synkope. Revaskularisering ved kendt iskæmisk hjertesygdom uden nyt infarkt vil sjældent reducere ventrikulær arytmibyrde. Patienten skal derfor være i optimal medicinsk behandling inkl. maksimal tolerabel betablokker. ICD indikation kan i udvalgte tilfælde vejledes af en elektrofysiologisk undersøgelse.
Non-sustained VT/PVC: hvis Holter dokumenterer symptomatisk hyppig PVC/VT trods medicinsk behandling (verapamil/flecainid eller betablokker for hhv. hvile- og aktivitetsudløst PVC/VT), anbefales ablation. Symptomatisk PVC/VT særligt fra højre ventrikels udløbsdel (LBBB morfologi, inferior akse) men også venstre fascikulær PVC/VT (RBBB, superior akse) behandles mere effektiv med ablation, og ablation skal derfor tilbydes patienten efter information om høj behandlingseffektivitet og lav procedurerisiko. Patienten bør tilbydes muligheden for at afprøve mindre effektiv medicinsk behandling før ablation, hvis dette ønskes (gøres typisk også i ventetiden på ablation). Ved tvivl om PVC lokalisation konfereres EKG og behandlingsmulighederne med HSE. Asymptomatiske patienter med høj PVC-byrde (>10%) uden hjertesvigt anbefales årlige kliniske og ekkokardiografi kontroller mhp. venstre ventrikel dilatation og/eller fald i LVEF.
Patienter med anden non-iskæmisk kardiomyopati: patienter med dilateret kardiomyopati og hjertesvigt med LVEF ≤35% er potentielle kandidater til ICD, se Kapitel 20: Implanterbar cardioverter defibrillator (ICD), Afsnit 20.2.
ICD bør ligeledes overvejes hos disse patienter ved LVEF <50% omend et evtl. udredningsprogram med hjerte-MR og elektrofysiologisk undersøgelse skal guides af alder, familiær disposition og symptomer.
I de sjældne tilfælde, hvor arvelighed mistænkes, kan klinik for arvelige hjertesygdomme rådføres iht. Kapitel 32: Arvelige hjertesygdomme.
Medicinsk behandling og ICD-indikation afklares på HSE.
Patienter med sjældne årsager til ventrikulær arytmi
Nedenfor er en kort operationel oversigt over behandling af sjældne men potentielt livstruende ventrikulær arytmi.
- Brugada syndrom: quinidin (iskæmisk hjertesygdom eller hjertesvigt kontraindicerer behandlingen) evt. forudgået af i.v. isoprenalin (ventrikel frekvens 80-100 per min). Quinidin kan kun udskrives efter særlig ansøgning og behandlingen varetages på HSE. ICD er indiceret.
- Katekolaminerg polymorf VT (CPVT): betablokkere er førstevalg og konkurrencesport frarådes. Flecainid som tillæg kan forsøges når betablokkere har utilstrækkelig effekt. Hjertestopsoverlevere anbefales ICD. Behandlingen varetages på HSE.
- Kort-koblet PVC udløst VF: Konferer med HSE angående ablation og/eller Quinidin. Alternativt kan anvendes verapamil, men der er mindre evidens for effekt ved langtidsbehandling. Betablokker behandling synes ineffektiv.
- Erhvervet langt QT-syndrom med torsades-de-pointes (TdP)-VT/VF: elektrolytstatus kontrolleres og K+ >4,0mmol/l og Mg++ >0,80 mmol/l tilstræbes ved bolus/infusion. Isoprenalininfusion til QRS-frekvens på ca. 80-100/min eller forbigående hurtig pacing (ca. 80-100/min.) enten via temporært pace-kateter/ledning eller via et i forvejen implanteret permanent device (PM eller ICD). Seponering af farmaka med QT-forlængende effekt.
- Medfødt langt QT-syndrom: betablokker behandling er indiceret. Behandlingen varetages på HSE
- Polymorf VT/VF: overvej akut KAG, da iskæmi er en hyppig årsag til forlænget QT og PVC, hvorved risikoen for polymorf VT/VF øges. Sammenligning af aktuelt EKG med tidligere EKG kan bidrage til bagvedliggende ætiologi (fx iskæmi eller langt QT-syndrom). Kaliumsubstitution ved hypokaliæmi, magnesiumsulfat i.v. Ved bradykardiudløst (fx avanceret AV blok) VT/VF anbefales temporær pacing (ca. 80-100/min.) enten via temporært pace-kateter/ledning eller via et evt. permanent device (PM eller ICD). Overvej radiofrekvensablation særligt, hvis trigger er hyppige monomorf PVC.
18.6 Telemetri hos patienter med elektrolytforstyrrelser
Ved moderat til svær elektrolytforstyrrelse er der en øget arytmirisiko både i form af VT, bl.a. torsades de pointes VT, og betydende bradyarytmier med risiko for synkope og klinisk hjertestop. Arytmirisiko for den enkelte patient afhænger af en kompleks kombination af flere faktorer (arytmi-substrater og arytmi-triggere):
- eksisterende hjertesygdom (fx hjertesvigt eller ionkanalsygdom)
- komorbiditet, herunder syrebase-status (fx svigtende respiration og kredsløb)
- medicinsk behandling (fx digoxin ved hypokaliæmi)
- hastigheden af udviklingen af elektrolytforstyrrelsen (akutte forandringer tolereres generelt dårligere end kroniske)
- udvikling af typiske kliniske symptomer (fx muskelsvaghed ved kaliumforstyrrelse)
- udvikling af typiske elektrokardiografiske forandringer (specifik for typen af elektrolytforstyrrelse)
Svær kaliumforstyrrelse udgør i klinisk praksis den største gruppe af patienter med risiko for betydende arytmier. Indikationen for telemetri afhænger ved både hypo- og hyperkaliæmi af en samlet klinisk vurdering med anamnese, objektiv undersøgelse, og EKG-12.
Trods forstyrrelser i calcium og magnesium kan give EKG-forandringer og dermed risiko for betydende arytmi, foreslås ikke håndfaste anbefalinger herom, da arytmirisikoen og dermed telemetribehovet for disse elektrolytforstyrrelser er mere sparsomt beskrevet i litteraturen. Imidlertid virker det rimeligt, at der følges samme principper som for kaliumforstyrrelser med en samlet vurdering af den målte værdi og den kliniske præsentation.
Hypokaliæmi (K+ <3,5 mmol/L)
- kan give anledning til taky- og bradyarytmier med synkope eller hjertestop
- EKG-forandringer: typisk prominent U-tak, affladet T-tak, og ST-deviation
- telemetri:
- indiceret ved isoleret meget svært nedsat K+ <2,0 mmol/L. Digoxin bør pauseres ved svær hypokaliæmi.
- svær (K+ <2,5 mmol/L) til moderat (K+ 2,5-2,9 mmol/L) hypokaliæmi med relevante ekg-forandringer og/eller kliniske symptomer såsom muskelsvaghed, hypokaliæmi-inducerede arytmier, og/eller tilstande med prædisposition til arytmier ved hypokaliæmi fx digoxinbehandling, hjertesvigt, iskæmisk hjertesygdom, (især akut koronart syndrom), AV-blok, og langt QT-syndrom
Hyperkaliæmi (K+ >5,5 mmol/L)
- kan give anledning til taky- og bradyarytmier med synkope eller hjertestop
- EKG-forandringer: 1. grads AV-blok, affladede eller manglende P-takker, høje spidse T-takker (T-tak > R-tak i > 1 afledning), ST-depression, sammensmeltning af S-tak og T-tak, bredde QRS-komplekser, VT og bradykardi.
- telemetri:
- bør udføres ved svær hyperkaliæmi (K+ ≥6,5 mmol/L)
- overvejes ved lavere kalium, særligt ved hurtigt udviklet hyperkaliæmi, typiske EKG-forandringer, kliniske symptomer med muskelsvaghed, og hyperkaliæmi-inducerede arytmier.
For en kort operationel oversigt over den medicinske akutte behandling af betydende elektrolytforstyrrelser henvises til afsnit om ”special circumstances” i nyeste ALS-guidelines fra det Europæiske Råd for Genoplivning, oktober 2021.