13. Pulmonal hypertension
13.1 Definition og klassifikation
Pulmonal hypertension (PH) er et syndrom forårsaget af øget modstand i lungekredsløbet, som medfører øget tryk og ultimativt højre ventrikelsvigt. PH defineres som et forhøjet pulmonalarteriemiddeltryk (mPAP) >20mmHg i hvile, målt ved højresidig hjertekateterisation. Normalt er mPAP i hvile 14 ± 3mmHg. Hæmodynamisk inddeles PH i præ-kapillær PH og post-kapillær PH baseret på måling af pulmonalarterie indkilingstrykket (PAWP). Lungekarmodstanden (PVR) har enheden Wood Units og beregnes som den transpulmonale gradient (TPG: mPAP-PAWP) divideret med cardiac output (CO). PVR er normalt <2 Wood Units.
PH betegner en hæmodynamisk og patofysiologisk tilstand, der optræder i flere forskellige kliniske sammenhænge og inddeles i 5 forskellige grupper (Tabel 13.1). Behandlingsprincipper i de fem grupper er ikke ens. Specielt kan specifik pulmonal vasodilaterende behandling, som anvendes ved gruppe 1 PAH, være direkte kontraindiceret i andre grupper. Korrekt klassifikation af den enkelte patient er derfor afgørende for at sikre den rette behandling.
Tabel 13.1. Klinisk klassifikation af pulmonal hypertension | |
Gruppe 1. Pulmonal arteriel hypertension (PAH) | |
|---|---|
1.1 Idiopatisk (IPAH) 1.2 Hereditær (HPAH; BMPR2 mutation eller andre mutationer) 1.3 Farmaka eller toxin induceret 1.4 Associeret PAH (APAH; bindevævssygdom, HIV-infektion, portal hypertension, kongenit hjertesygdom, schistosomiasis) 1.5 PAH med langtidseffekt af calciumkanalblokkere 1.6 Pulmonal veneokklusionssygdom og/eller pulmonal kapillær hæmangiomatose | |
Gruppe 2. Pulmonal hypertension ved venstresidig hjertesygdom (Systolisk -, diastolisk hjertesvigt, klapsygdom mm.) | |
Gruppe 3. Pulmonal hypertension ved lungesygdom og/eller hypoksæmi | |
Gruppe 4. Kronisk tromboembolisk pulmonal hypertension (CTEPH) og andre pulmonalarterie obstruktioner | |
Gruppe 5. PH med uklar og/eller multifaktoriel mekanisme (sarkoidose, myeloproliferative tilstande | |
13.2 Forekomst
- i europæiske lande er incidensen af PAH 5-10/million/år og prævalensen 45-55/million. I det danske PH register (DAN-PH) er incidensen og prævalensen henholdsvis 7/million/år og 50/million
- PAH diagnosticeres med stigende alder ofte >60 år og i tiltagende grad ligeligt fordelt mellem køn, betinget af stigende komobiditeter
- i den generelle befolkning ses PH langt hyppigst sekundært til venstresidig hjertesygdom eller lungesygdom (gruppe II og III)
- incidensen af kronisk tromboembolisk pulmonal hypertension (CTEPH) er i DAN-PH registret til 7/million/år
13.3 Diagnostik og undersøgelser
Diagnosen PH stilles desværre ofte sent i sygdomsforløbet med en forsinkelse på to til tre år fra symptomdebut og bør overvejes hos alle patienter med relevante symptomer. Specielt skal man være opmærksom på patienter, der er i øget risiko for udvikling af PAH (arvelig disposition, medfødte hjertesygdomme, HIV, portal hypertension eller bindevævssygdom, herunder især sklerodermi og systemisk lupus erythematosus) og mistænke kronisk tromboembolisk pulmonal hypertension (CTEPH) ved funktionsnedsættelse efter tidligere akut lungeemboli.
Påvisning af pulmonal hypertension
Symptomerne ved PH er uspecifikke, udløses i begyndelsen ved anstrengelse og omfatter:
- dyspnø
- øget trætbarhed
- nedsat fysisk funktionsevne
Senere optræder
- angina (højre ventrikel iskæmi)
- anstrengelsesrelaterede nærsynkoper/synkoper
- tegn på højresidigt hjertesvigt (halsvenestase, hepatomegali, pleuravæske, ascites, underekstremitetsødemer)
Anamnesen bør indeholde oplysninger om mulige risikofaktorer som:
- familiær disposition
- brug af slankemidler
- bindevævssygdom
- leversygdom
- HIV-infektion
- kronisk lungesygdom
- venstresidig hjertesygdom, herunder risikofaktorer til hjertesvigt
- tidligere episoder med venøs tromboembolisme
Funktionsniveauet hos patienter med PAH angives som WHO-klasse I-IV (svarer til NYHA klassifikationen ved hjerteinsufficiens).
Objektiv undersøgelse
- hjertestetoskopi: accentueret 2. hjertelyd og uddrivningsmislyd over pulmonalen. Eventuelt systolisk insufficiensmislyd over tricuspidalen og diastolisk regurgitationsmislyd over pulmonalen
- ved manifest højresidigt hjertesvigt ses halsvenestase, leverforstørrelse samt perifere ødemer. Der undersøges for bindevævssygdom, cyanose og trommestikfingre
- EKG: ofte højresidig akse og hypertrofi og eventuelt højresidigt grenblok
- røntgen af thorax: hjerteektasi og forstørrede centrale pulmonalarterier ved fremskredne tilfælde af PH
- funktionskapaciteten kvantiteres ved 6-min. gangtest, der udføres med samtidig pulsoximetri
Undersøgelsesprogrammet ved mistanke om PH indeholder typisk transthorakal ekkokardiografi (TTE) som screeningsundersøgelse. Ved screeningsverificeret PH suppleres med undersøgelser, der karakteriserer typen af PH og dermed behandlingsmuligheder for pulmonal hypertension, udover behandling af eventuel grundsygdom (Figur 1).
| Figur 13.1: Udredningsprogrammet ved mistanke om PH. |
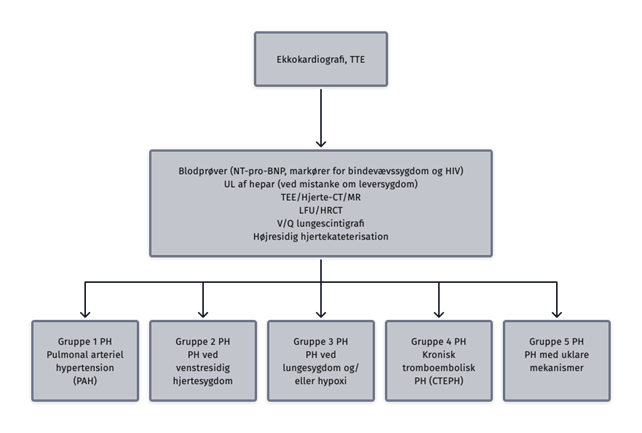 |
| TTE: transthorakal ekkokardiografi; NT-proBNP: N-terminal pro-Brain Natriuretic Peptide; UL: ultralydsundersøgelse af leveren (ved mistanke om leversygdom); TEE: transoesophageal ekkokardiografi; LFU: lungefunktions undersøgelse; HRCT: High Resolution CT; V/Q lungeskintigrafi: ventilations-perfusions lungeskintigrafi. |
Transthorakal ekkokardiografi (TTE)
Er vigtig som screening for PH. En tricuspidalklap returgradient (TRG) >40 mmHg angiver høj sandsynlighed for PH, men PH bør også overvejes ved lavere TRG, hvis der samtidigt er andre ekkokardiografiske tegn på højre ventrikel (RV) belastning:
- højre ventrikel:
- dilatation (RV er større end venstre ventrikel (LV) i apikalt 4-kammer billede)
- hypertrofi (vægtykkelse >5mm)
- nedsat systolisk funktion: Tricuspid Annular Plane Systolic Excursion (TAPSE) ≤1,8cm
- deviation af ventrikelseptum og atrieseptum mod venstre
- pulmonal arterie:
- dilatation (>25mm)
- forkortet pulmonal arteriel accelerationstid (<105ms og/eller midtsystolisk ”notch”)
- pulmonalklapinsufficiens med forhøjet tidlig regurgitationshastighed (>2.2m/s)
- højre atrium:
- forstørrelse (>18cm2)
- dilatation af vena cava inferior og centrale pulmonalarterier
- perikardium: ved svær PH og RV svigt ses ofte en mindre perikardieeffusion (perikardievenerne drænerer via centrale vener til højre atrium)
Bestemmelse af typen af pulmonal hypertension
- ved TTE undersøges også for venstresidig hjertesygdom. Et dilateret venstre atrium kan udtrykke underliggende diastolisk LV dysfunktion/hypertensiv hjertesygdom, som er en hyppig årsag til PH hos ældre. Der undersøges desuden for medfødt hjertefejl med shunt (eventuelt kan suppleres med kontrastekkokardiografi, transesophageal ekkokardiografi (TEE), hjerte-CT eller hjerte-MR). Sinus venosus atrieseptumdefekt, partielt abnormt indmundende lungevener og aortopulmonalt vindue kan let overses ved TTE
- lungefunktionsundersøgelse og arterielle gastensioner udføres som screening for kronisk lungesygdom. Ved mistanke om interstitiel lungesygdom udføres high-resolution CT-scanning. PAH og CTEPH medfører restriktiv forstyrrelse i lungevolumina og nedsat diffusionskapacitet. Ved PAH ses let til højest moderat hypoxæmi (iltmætninger ofte > 90%) og normalt eller nedsat PaCO2. Under anstrengelse er der tendens til desaturation
- ventilations-perfusions lungeskintigrafi viser ved CTEPH segmentære og/eller lobære perfusionsdefekter, og en normal undersøgelse udelukker med stor sandsynlighed tromboembolisk årsag. CT-lungeangiografi er også af værdi ved CTEPH, men en tilsyneladende normal undersøgelse udelukker ikke med tilstrækkelig sikkerhed CTEPH
- ved mistanke om APAH kan bestemmelse af antinukleære antistoffer og HIV-antistoffer være indiceret
- ultralydsskanning af leveren udføres ved mistanke om leversygdom og portopulmonal hypertension
Højresidig hjertekateterisation
Foretages med henblik på:
- definitivt at stille diagnosen PH og at bidrage til typebestemmelsen af PH
- at fastlægge sygdommens sværhedsgrad
- at teste pulmonalkredsløbets vasoreaktivitet
PH inddeles i præ-kapillær, post-kapillær eller kombineret i henhold til Tabel 13.2. Ved visse former af præ-kapillær PH undersøges lungekredsløbets akutte vasoreaktivitet ved en pulmonal vasodilatationstest overfor inhaleret nitrogen oxid (NO). Patienter med CTEPH undersøges med selektiv pulmonalangiografi.
Definition | Hæmodynamik |
|---|---|
PH | mPAP ≥20mmHg |
Præ-kapillær PH | mPAP >20mmHg |
Post-kapillær PH | mPAP >20mmHg |
Kombineret post-kapillær og | mPAP >20mmHg |
13.4 Prognose
- naturhistorien ved PH er karakteriseret ved gradvist tiltagende lungekarmodstand og RV dysfunktion. Prognosen er tæt korreleret til graden af RV-dysfunktion
- ubehandlet er prognosen for IPAH alvorlig med overlevelse efter 1, 3 og 5 år omkring 70%, 50% og 35%
- efter indførelse af moderne farmakologisk PAH-behandling er overlevelsen markant forbedret med overlevelse efter 5 år >90 %
For den enkelte patient med PAH indikerer følgende parametre en dårlig prognose:
- WHO-funktionsklasse >II, 6-min gangtest <300m, maksimal iltoptagelse (VO2 max) <12 ml/kg/min
- TAPSE <1,5cm, perikardieeffusion ved ekkokardiografi
- trykket i højre atrium (RAP) >15mmHg, CI <2.0 l/min/m2, fravær af signifikant vasoreaktivitet overfor inhaleret NO ved højresidig hjertekateterisation
- forhøjet BNP >180pg/ml, NT-proBNP >1400pg/ml
Prognosen ved CTEPH er lige så alvorlig som ved PAH. Vellykket kirurgisk pulmonal endarterektomi (PEA) medfører en markant forbedring af prognosen.
13.5 Visitation
- TTE/TEE, lungefunktionsundersøgelse, ventilations-perfusions lungeskintigrafi og undersøgelse for mulig bindevævssygdom, HIV-infektion eller portal hypertension kan foregå ved funktionsbærende enheder i kardiologi i samarbejde med de relevante specialer (reumatologi og lungemedicin)
- patienter med PH (TRG >40mmHg og/eller andre ekkokardiografiske tegn på PH) med symptomer som skønnes forårsaget af PH, henvises til højtspecialiseret center for PH m.h.p. definitiv diagnostik, hvilket ofte vil inkludere højresidig hjertekateterisation
- patienter med PH som er velforklaret ud fra lungesygdom eller venstresidig hjertesygdom kræver sædvanligvis ikke henvisning til PH-center, men det skal overvejes ved usikkerhed om årsagen (typen af PH) eller ved PH i en sværhedsgrad der ikke er forventet ud fra den underliggende sygdom
- specifik medicinsk behandling for PAH initieres og kontrolleres i højtspecialiseret center for PH. Funktionsbærende enheder i kardiologi kan inddrages i kontrollen efter aftale med det højtspecialiserede center
- patienter med PAH, WHO-klasse III-IV og svigt af specifik farmakologisk behandling vurderes med henblik på lungetransplantation (DLTX) som foretages på Rigshospitalet
- patienter som mistænkes for CTEPH (segmentære og/eller lobære perfusionsdefekter ved ventilations-perfusions lungeskintigrafi) og er i WHO-funktionsklasse II-IV, henvises til udredning med henblik på PEA eller ballon pulmonal angioplastik (BPA)
- patienter som mistænkes for PAH på baggrund af kongenit hjertesygdom, henvises til landsdelsafdeling i kardiologi med børnekardiologisk specialfunktion
13.6 Generelle anbefalinger
- PAH medicin bør ikke ændres ved anden akut sygdom uden konference med PH-center
- fysisk træning anbefales inden for symptomgrænserne. Fysiske træningsprogrammer/rehabilitering kan forbedre patienternes funktionsevne. Hård fysisk aktivitet med udvikling af svær åndenød, svimmelhed eller brystsmerter frarådes
- som hovedregel kontraindicerer PH graviditet. Afbrydelse af svangerskabet tilrådes ved opstået graviditet
- PH-patienter i WHO-klasse II-III tåler normalt flyvning uden problemer. Ilt kan tilbydes ved henvendelse til flyselskabet – skal bestilles sammen med flybilletten. WHO-klasse IV patienter bør ledsages af læge under flyvning
- PH forøger risikoen ved generel anæstesi og kirurgi. Større indgreb i general anæstesi bør udføres på PH-center med mulighed for hæmodynamisk monitorering samt administration af NO og prostanoider
vaccination imod COVID-19, influenza og pneumokokpneumoni anbefales
13.7 Uspecifik farmakologisk behandling af PH
- diuretika: anvendes ved manifest højresidig hjerteinsufficiens (perifere ødemer og/eller ascites). Sædvanligvis anvendes loop diuretika i kombination med spironolakton
- llt-behandling: betydende hypoxæmi bør behandles med kontinuerlig ilt (hjemme-ilt), såfremt iltmætningen er <90%. Modvirker hypoksisk pulmonal vasokonstriktion
13.8 Specifik farmakologisk behandling af PAH
PDE-5-hæmmere/sGC stimulator
Tadalafil og Sildenafil er Phospherdiesterase-5-hæmmere til anvendelse ved PAH WHO klasse II-III . Bivirkningerne omfatter hovedpine, synsforstyrrelser og gastrointestinale symptomer. Anvendes i dag typisk som førstevalg.
Riociguat er en stimulator af opløseligt guanylat cyklase (sGC), der efterligner virkningen af NO og forøger cGMP i bl.a. pulmonalarteriernes glatte muskelceller. Det forbedrer symptomer og prognose ved PAH og CTEPH (WHO funktionsklasse II-IV). Administreres oralt. Bivirkningerne omfatter hovedpine, synsforstyrrelser og gastrointestinalesymptomer.
Endothelinreceptor-antagonister
Endothelin fremkalder vasokonstriktion og celleproliferation i pulmonalkredsløbet, begge dele modvirkes af endothelinreceptor-antagonister til PAH-patienter i WHO funktionsklasse II-IV. Bivirkninger omfatter flushing, vægtstigning, væskeretention, ødemer, fald i hæmoglobin, hæmning af hormonal antikonception, teratogenicitet og måske mandlig infertilitet.
Bosentan er en kompetitiv blokker af endothelin ETA og ETB-receptorer. Administreres oralt. Forbedrer symptomer, hæmodynamik og prognose for PAH-patienter i WHO funktionsklasse II-IV. Reversibel leverpåvirkning (forhøjede transaminaser) optræder hos 10%. Behandlingen kræver regelmæssig monitorering af leverfunktionsparametrene i hele behandlingsperioden.
Ambrisentan har færre interaktioner end bosentan, men kræver også jævnlig monitorering af leverparametre. Særligt fald i hæmoglobin kan optræde (ukendt mekanisme).
Macitentan er mindre levertoxisk end bosentan og færre interaktioner. Særligt fald i hæmoglobin kan optræde (ukendt mekanisme).
Prostanoider
Prostanoider forøger cAMP intracellulært og medfører pulmonal vasorelaksation, hæmning af celleproliferation i pulmonalarterierne, inotrop stimulation af RV samt hæmning af trombocytaggregationen.
Epoprostenol (syntetisk prostacyclin) anvendes til behandling af PAH-patienter i WHO-funktionsklasse III-IV. Pga. kort halveringstid (½-3 min.) er kontinuerlig infusion i et tunneleret centralt venekateter via bærbar infusionspumpe nødvendig. Ved svigt af infusionssystemet er der risiko for alvorlig rebound-PAH.
Øvrige bivirkninger omfatter kateterinfektion/sepsis, vasodilatation, hypotension, takykardi, flushing, hovedpine, kvalme, opkastning, kolik og kæbesmerter.
Treprostinil er et prostanoid med længere halveringstid end både epoprostenol og iloprost. Kan anvendes som kontinuerlig subkutan eller intravenøs infusion. Lægemidlet fremkalder individuelt varierende grader af inflammation i huden, hvilket begrænser stoffets anvendelse til subkutan infusion. Treprostinil kan administreres intravenøst via en ekstern pumpe eller en implanterbar infusionspumpe (LenusPro), der indopereres under huden.
Iloprost har en længere halveringstid på 30 min. Kan anvendes som inhalation og kræver 6-9 inhalationer dgl. via et kompakt ultralydsdrevet inhalationsudstyr (4-5 min. pr. inhalation). Færre bivirkninger fra systemkredsløbet (pulmonal selektivitet). Anvendes ofte i kombination med oral sildenafil, som forstærker virkningen. Kan også anvendes intravenøst via bærbar infusionspumpe.
Selexipag er en oralt aktiv IP prostacyclinreceptor-agonist, der reducerer sygdomsprogression og hospitalisering ved PAH. Det er også virksomt hos PAH patienter, som i forvejen er i behandling med endothelinreceptor-antagonister eller fosfodiesterase-5 (PDE-5) -hæmmere, men har ikke vist supplerende effekt ved allerede iværksat dobbeltbehandling med endothelinreceptor-antagonister og PDE-5-hæmmere på det primære endepunkt, pulmonal vaskulær modstand.
Calciumantagonister
Calciumantagonister bør aldrig anvendes, medmindre der er påvist signifikant reversibilitet ved en pulmonal vasodilatationstest overfor NO ved højresidig hjertekateterisation. Er der positiv vasodilatationstest, kan patienten behandles med dihydropyridin-calciumantagonist alene (højst 10% og ved en længere tidshorisont 5% af patienterne). Patienter med PAH og negativ vasoreaktivitetstest har risiko for hæmodynamisk kollaps ved behandling med calciumantagonister pga. negativ inotrop effekt og systemisk vasodilatation.
Nitroglycerin, nitroprussid og nicorandil er kontraindicerede under behandling med PDE-5- hæmmere eller riociguat. Riociguat og PDE-5-hæmmere må ikke kombineres pga. risiko for hypotension.
Behandlingsmål og monitorering
Virkningen af den medicinske behandling rettet mod PAH kontrolleres hos den enkelte patient med WHO-funktionsklasse, 6-min. gangtest, TTE og hæmodynamik (højresidig hjertekateterisation). Det tilstræbes, at patienter opnår WHO funktionsklasse I-II, en 6-min. gangtest over 440 m og fravær af RV-svigt.
Kombinationsbehandling hos patienter med PAH
Flere undersøgelser har vist positiv effekt ved kombination af specifikke farmaka for PAH med forskellige virkningsmekanismer (endothelin-blokker, PDE-5-hæmmer/sGC stimulator, prostanoid). Mange PAH-patienter er i 2-stofs- og et stigende antal i 3-stofsbehandling.
Specifikke PAH farmaka ved PH-gruppe 2, og 3
Der er ingen evidens for gavnlig virkning af specifikke PAH-midler ved PH relateret til venstresidig hjertesygdom eller lungesygdom (PH-gruppe 2 og 3), fraset at inhaleret treprostinil forbedrer 6-min. gangtest, reducerer NT-proBNP og reducerer risiko for klinisk progression ved PH relateret til interstitiel lungesygdom. Behandlingen forventes ikke indført i Danmark med nuværende evidensniveau. Der er vist direkte forværring af sygdom ved brug af riociguat og ambrisentan ved interstitiel lungesygdom eller KOL og ved macitentan og sildenafil ved PH sekundært til venstre ventrikel sygdom.
Brug af PAH farmaka ved behandling af CTEPH (PH-gruppe 4)
Riociguat er vist at forbedre symptomer og funktionsevne i denne patientgruppe. Der en vis klinisk erfaring med andre specifikke farmaka for PAH specielt PDE-5-hæmmere, men der mangler systematisk dokumentation af effekten.
13.9 Lungetransplantation
- patienter med PAH, WHO klasse III-IV og svigt af maksimal farmakologisk behandling bør henvises til vurdering med henblik på dobbelt lungetransplantation (DLTX), Rigshospitalet
13.10 Kronisk tromboembolisk pulmonal hypertension
Risikoen for udvikling af CTEPH efter akut lungeemboli er omkring 2-4% og kun 50-75% af patienter med CTEPH har haft verificerede tilfælde af venøs tromboembolisme. Prognosen er alvorlig og patienter i WHO-klasse II-IV skal henvises til invasiv udredning og vurdering med henblik på evt. intervention (højresidig hjertekateterisation og selektiv pulmonalangiografi). Udredning foregår på PH-centrene. PEA og BPA-behandling for CTEPH foregår på Aarhus Universitetshospital (AUH).
Behandlingen er multimodal og har som oftest har eklatant virkning på den pulmonale hæmodynamik, symptomer og overlevelse. For nogle patienter er (pulmonal endarterektomi) førstevalg. Den perioperative mortalitet på AUH er lav med ca. 2%. Patienter der er inoperable eller har rest PH efter PEA kan ofte tilbydes ballon pulmonal angioplasti (BPA). Ved fortsat PH kan man overveje specifik pulmonal vasodilaterende behandling som nævnt i afsnit 13.8.
Alle patienter med CTEPH behandles med livslang AK-behandling (Vitamin K antagonist (VKA) med INR 2-3). Der bruges primært VKA men NOAK kan overvejes.
Såfremt der i anamnesen er akut lungeemboli, bør patienterne på undersøgelsestidspunktet have været i behandling med marevan i mindst 3 måneder efter den akutte episode (trombematerialet skal være organiseret/fibroseret på operationstidspunktet).
Høj TRG ≥ 50 mmHg ved den akutte lunge emboli giver mistanke om mere kronisk højre ventrikel belastning, og henvisning til PH-center kan overvejes tidligere.


